





Estude fácil! Tem muito documento disponível na Docsity

Ganhe pontos ajudando outros esrudantes ou compre um plano Premium


Prepare-se para as provas
Estude fácil! Tem muito documento disponível na Docsity
Prepare-se para as provas com trabalhos de outros alunos como você, aqui na Docsity
Os melhores documentos à venda: Trabalhos de alunos formados
Prepare-se com as videoaulas e exercícios resolvidos criados a partir da grade da sua Universidade
Responda perguntas de provas passadas e avalie sua preparação.

Ganhe pontos para baixar
Ganhe pontos ajudando outros esrudantes ou compre um plano Premium
Comunidade
Peça ajuda à comunidade e tire suas dúvidas relacionadas ao estudo
Descubra as melhores universidades em seu país de acordo com os usuários da Docsity
Guias grátis
Baixe gratuitamente nossos guias de estudo, métodos para diminuir a ansiedade, dicas de TCC preparadas pelos professores da Docsity
Resumo de fisiologia da fertilização
Tipologia: Resumos
Compartilhado em 02/11/2019
5
(3)8 documentos
1 / 11

Esta página não é visível na pré-visualização
Não perca as partes importantes!







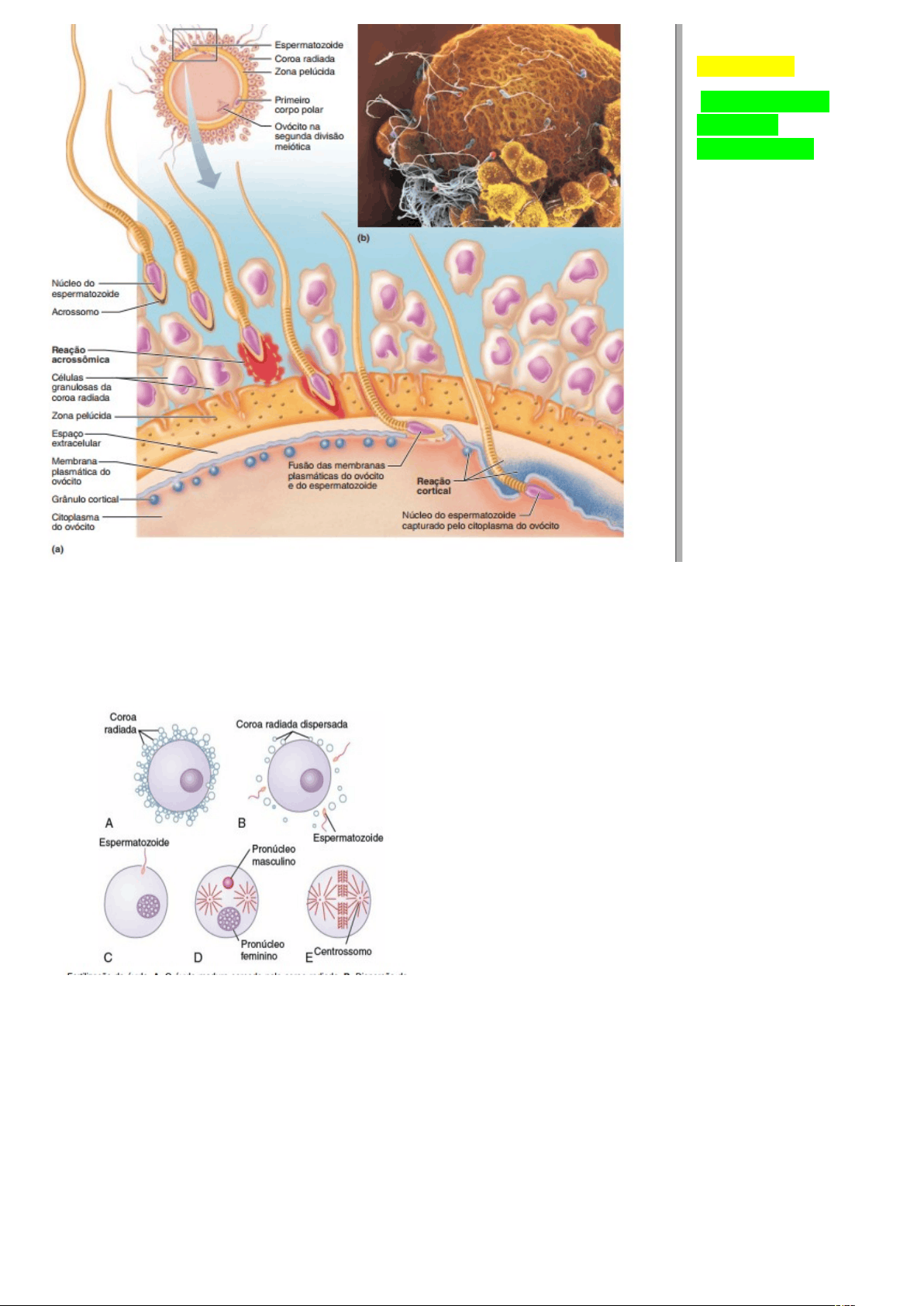
FERTILIZAÇÃO Eventos que levam à fertilização Antes que a fertilização possa ocorrer, os espermatozoides depositados na vagina precisam nadar através do útero para alcançar o ovócito recém- ovulado na tuba uterina. Sabe-se que os espermatozoides têm proteínas denominadas receptores olfatórios , que respondem a estímulos químicos. Depois que o homem ejacula sêmen na vagina da mulher durante a relação sexual, alguns espermatozoides são transportados, de 5 a 10 minutos, na direção ascendente da vagina e através do útero e das trompas de Falópio até as ampolas das trompas de Falópio, próximas às terminações ovarianas das trompas. Esse transporte dos espermatozoides é auxiliado por contrações do útero e das trompas de Falópio, estimuladas por prostaglandinas no líquido seminal masculino e também por ocitocina liberada pela hipófise posterior da mulher durante o seu orgasmo. A fertilização do óvulo ocorre normalmente na ampola de uma das trompas de Falópio, pouco depois de o espermatozoide e o óvulo entrarem na ampola. Entretanto, antes que o espermatozoide consiga entrar no óvulo, ele precisa primeiro penetrar as múltiplas camadas de células da granulosa anexadas ao exterior do óvulo (a coroa radiada ) e, em seguida, se fixar e penetrar a zona pelúcida que circunda o óvulo. Depois que o espermatozoide chega ao ovócito, ele liga-se aos receptores na zona pelúcida em volta do ovócito e sofre uma reação acrossômica , a liberação de enzimas digestivas do seu acrossomo. Essas enzimas digerem uma fenda na zona, através da qual o espermatozoide ziguezagueia para chegar Ao óvulo. A membrana plasmática de um único espermatozoide funde-se com a membrana plasmática do ovócito e o núcleo do espermatozoide é capturado pelo citoplasma do ovócito. Essa fusão induz a reação cortical : grânulos no ovócito secretam enzimas no espaço extracelular abaixo da zona pelúcida. Essas enzimas alteram a zona pelúcida e destroem os receptores de espermatozoides, impedindo que qualquer outro espermatozoide se ligue e entre no ovo Uma vez que o espermatozoide tenha entrado no óvulo (que ainda se encontra no estágio de desenvolvimento de oócito secundário), o oócito se divide mais uma vez, formando o óvulo
maduro , mais um segundo corpo polar , que é expelido. O óvulo maduro ainda carrega em seu núcleo (agora denominado pronúcleo feminino ) 23 cromossomos. O TRANSPORTE DO OVO FERTILIZADO NA TROMPA DE FALÓPIO Depois de ocorrida a fertilização, normalmente são necessários outros 3 a 5 dias para o transporte do ovo fertilizado pelo restante da trompa de Falópio até a cavidade uterina. Esse transporte é feito, basicamente, pela fraca corrente de líquido na trompa, decorrente da secreção epitelial mais a ação do epitélio ciliado que reveste a trompa; os cílios sempre batem na direção do útero. Contrações fracas da trompa de Falópio também podem ajudar a passagem do ovo. Esse transporte lento do ovo fertilizado pela trompa de Falópio permite a ocorrência de diversos estágios de divisão celular antes que ele — agora denominado blastocisto, com cerca de 100 células — entre no útero. Durante esse tempo, as células secretoras da trompa de Falópio produzem grande quantidade de secreções usadas para nutrir o blastocisto em desenvolvimento. A IMPLANTAÇÃO DO BLASTOCISTO NO ÚTERO Após chegar ao útero, o blastocisto flutua livremente na cavidade uterina por dois dias, recebendo nutrientes das secreções uterinas. Durante esse período, ele permanece “incubado”, digerindo parte da zona pelúcida para criar uma grande abertura e se espremer através dela. Cerca de seis dias após a fertilização, o blastocisto começa a implantação , que é o ato de penetrar no endométrio. A implantação resulta da ação de células trofoblásticas que se desenvolvem na superfície do blastocisto. Essas células secretam enzimas proteolíticas que digerem e liquefazem as células adjacentes do endométrio uterino. Parte do líquido e dos nutrientes liberados é transportada ativamente pelas mesmas células trofoblásticas no blastocisto, dando mais sustento ao crescimento. A mostra um blastocisto humano recém-implantado com pequeno embrião. Uma vez tendo ocorrido a implantação, as células trofoblásticas e outras células adjacentes (do blastocisto e do endométrio uterino) proliferam rapidamente, formando a placenta e as diversas membranas da gravidez. Nesse momento, o blastocisto consiste em uma massa celular interna (o futuro embrião) e em um trofoblasto externo (“gerador de alimentação”), uma camada que logo vai fornecer nutrição ao embrião a partir do útero materno. Na primeira etapa da implantação, as células do trofoblasto proliferam e formam duas camadas distinta. Uma camada interna, ou citotrofoblasto (“parte celular do trofoblasto”), onde ocorre a proliferação celular, e uma camada externa, ou sinciciotrofoblasto (“parte do trofoblasto com células fundidas”), onde as células perdem sua membrana plasmática e se fundem em uma massa multinucleada de citoplasma. O sinciciotrofoblasto projeta-se de modo invasivo no endométrio e digere as células uterinas com as quais entra em contato. À medida que o endométrio é erodido, o blastocisto fica profundamente
restante do embrião regridem e acabam desaparecendo. A parte do endométrio materno adjacente às complexas vilosidades coriônicas e ao cordão umbilical chama-se decídua basal , enquanto o endométrio oposto ao endométrio de decídua basal, no lado uterino-luminal do embrião implantado, é a decídua capsular. A decídua capsular expande-se para acomodar o embrião em crescimento, que se chama feto após o segundo mês, e enche completamente a luz uterina no início do quarto mês. Nesse quarto mês, a decídua basal e as vilosidades coriônicas perfazem, juntas, um disco espesso em forma de panqueca no final do cordão umbilical — a placenta —, que continua a nutrir o feto por mais seis meses, até o nascimento. Como ela se descola e desliza para fora do útero após o nascimento, o nome de sua porção materna — decídua (“a que cai”) — é adequado. Troca através da placenta As trocas que ocorrem através das vilosidades coriônicas entre o sangue materno e o fetal são absolutamente essenciais para a vida pré-natal. Essas trocas fornecem nutrientes e oxigênio ao feto, descartam seus resíduos e permitem que ele envie sinais hormonais para a mãe. Para viajar entre o sangue materno e o fetal, as substâncias precisam passar pela barreira placentária , que consiste nas três camadas de cada vilosidade coriônica sinciciotrofoblasto, citotrofoblasto, mesoderma extraembrionário. O sinciciotrofoblasto secreta muitas substâncias que chegam ao sangue materno e regulam os eventos da gravidez. Uma dessas substâncias é uma enzima que “desliga” os linfócitos T da mãe, evitando que seu sistema imune rejeite o feto. A maioria dessas substâncias, porém, é formada por hormônios. Alguns deles (progesterona e gonadotropina coriônica humana, ou HCG) mantêm o útero em seu estado de gravidez, e outros, secretados nos estágios finais da gravidez (estrogênios e hormônio de liberação da corticotropina), promovem o trabalho de parto. A produção do HCG começa logo depois da formação do sinciciotrofoblasto. PERMEABILIDADE PLACENTÁRIA E CONDUTÂNCIA POR DIFUSÃO NA MEMBRANA Nos primeiros meses de gravidez, a membrana placentária ainda é espessa porque não se desenvolveu completamente. Por conseguinte, sua permeabilidade é baixa. Além disso, a área superficial é pequena porque a placenta ainda não cresceu significativamente. Portanto, a condutância total por difusão é mínima, no primeiro momento. Por sua vez, mais tarde na gravidez, a permeabilidade aumenta devido ao afinamento das camadas de difusão da membrana e porque a área superficial se expande em muitas vezes, representando grande elevação na difusão placentária. A Difusão de Oxigênio Através da Membrana Placentária. O oxigênio, dissolvido no sangue dos grandes sinusoides maternos, passa para o sangue fetal por difusão simples , conduzido pelo gradiente de pressão do oxigênio do sangue materno para o sangue fetal. Perto do fim da gravidez, a média de pressão parcial de oxigênio (Po 2 ) do sangue materno nos sinusoides placentários fica em torno de 50 mmHg, e a média de Po 2 do sangue fetal, depois de oxigenado na placenta, é cerca de 30 mmHg. Portanto, o gradiente médio de pressão de difusão de oxigênio através da membrana placentária é de aproximadamente 20 mmHg. Isso significa que, com os níveis de Po 2 mais baixos no sangue fetal, a hemoglobina fetal consegue carregar 20% a 50% mais oxigênio do que consegue a hemoglobina materna. Em segundo lugar, a concentração de hemoglobina do sangue fetal é aproximadamente 50%
maior que a da mãe ; assim, tratando-se de um fator ainda mais importante para intensificar a quantidade de oxigênio transportada aos tecidos fetais. Em terceiro lugar, o efeito Bohr, a hemoglobina consegue carregar mais oxigênio com um nível de PCO baixo do que consegue com um nível de PCO 2 alto. O sangue fetal que entra na placenta carrega grande quantidade de dióxido de carbono, mas grande parte desse dióxido de carbono difunde-se do sangue fetal para o sangue materno. A Difusão de Dióxido de Carbono Através da Membrana Placentária. o único meio de excretar esse dióxido de carbono fetal é através da placenta para o sangue materno. A pressão parcial de dióxido de carbono (PCO 2 ) do sangue fetal é 2 a 3 mmHg maior que a do sangue materno. Esse pequeno gradiente pressórico do dióxido de carbono pela membrana é mais do que suficiente para permitir a difusão adequada do dióxido de carbono, porque a solubilidade extrema do dióxido de carbono na membrana placentária permite que ele se difunda cerca de 20 vezes mais rápido que o oxigênio. A Difusão de Nutrientes Através da Membrana Placentária. para fornecer esse alto nível de glicose, as células trofoblásticas que revestem as vilosidades placentárias proporcionam difusão facilitada de glicose através da membrana placentária, ou seja, a glicose é transportada por moléculas transportadoras nas células trofoblásticas da membrana. Devido à alta solubilidade dos ácidos graxos nas membranas celulares, eles também se difundem do sangue materno para o sangue fetal, porém mais lentamente do que a glicose, de modo que a glicose é usada mais facilmente pelo feto para sua nutrição. A Excreção de Resíduos Através da Membrana Placentária Da mesma maneira que o dióxido de carbono se difunde do sangue fetal para o sangue materno, outros produtos excretores formados no feto também se difundem através da membrana placentária para o sangue materno e, então, são excretados em conjunto com os produtos excretores da mãe. Eles incluem especialmente os produtos nitrogenados não proteicos, como ureia, ácido úrico e creatinina. O nível de ureia no sangue fetal é apenas ligeiramente maior que o do sangue materno porque a ureia se difunde através da membrana placentária com grande facilidade. A GONADOTROPINA CORIÔNICA HUMANA CAUSA PERSISTÊNCIA DO CORPO LÚTEO E EVITA A MENSTRUAÇÃO. A secreção desse hormônio pode primeiro ser medida no sangue, 8 a 9 dias após a ovulação, pouco depois do blastocisto se implantar no endométrio. Em seguida, a secreção aumenta rapidamente, atingindo nível
A hipófise anterior da mãe aumenta pelo menos 50% durante a gravidez e aumenta sua produção de corticotropina, tireotropina e prolactina. Por sua vez, a secreção hipofisária do hormônio foliculoestimulante e do hormônio luteinizante é quase totalmente suprimida, como consequência dos efeitos inibidores dos estrogênios e progesterona da placenta. Secreção de Corticosteroide Aumentada. A secreção adrenocortical de glicocorticoides fica, Geralmente, a gestante apresenta aumento de cerca de duas vezes na secreção de aldosterona, atingindo o pico no final da gravidez. Isto, em conjunto com as ações dos estrogênios, causa tendência, mesmo na gestante normal, de reabsorver o excesso de sódio de seus túbulos renais e, portanto, reter líquido, levando ocasionalmente à hipertensão induzida pela gravidez. Secreção da Glândula Tireoide Aumentada. A glândula tireoide materna aumenta, em geral, até 50% durante a gravi dez e eleva sua produção de tiroxina em quantidade correspondente. A maior produção de tiroxina é causada pelo menos parcialmente por efeito tireotrópico da gonadotropina coriônica humana, secretada pela placenta e por pequenas quantidades do hormônio específico estimulante da tireoide, a tireotropina coriônica humana, também secretada pela placenta. Secreção da Glândula Paratireoide Aumentada. As glândulas paratireoides maternas geralmente aumentam durante a gravidez; esse aumento é, sobretudo, verdadeiro se a mãe estiver sob dieta deficiente em cálcio. O aumento dessas glândulas causa absorção de cálcio dos ossos maternos, mantendo, assim, a concentração normal de íons cálcio no líquido extracelular materno, mesmo quando o feto remove cálcio para ossificar seus próprios ossos. Essa secreção do hormônio paratireóideo é ainda mais intensificada durante a lactação após o nascimento do bebê, porque o bebê em crescimento requer mais cálcio do que o feto. Secreção de “Relaxina” pelos Ovários e pela Placenta. Outra substância além dos estrogênios e da progesterona, um hormônio denominado relaxina, é secretada pelo corpo lúteo do ovário e pelos tecidos placentários. Sua secreção aumenta por efeito estimulador da gonadotropina coriônica humana, ao mesmo tempo em que o corpo lúteo e a placenta secretam grande quantidade de estrogênios e progesterona iva de energia para o metabolismo materno durante a gravidez. As Mudanças no Sistema Circulatório Materno Durante a Gravidez O Fluxo de Sangue Através da Placenta e o Débito Cardíaco Materno Aumentam Durante a Gravidez. Cerca de 625 mililitros de sangue fluem através da circulação materna da placenta a cada minuto, no último mês de gravidez. Esse fluxo, mais o aumento geral do metabolismo materno, aumenta o débito cardíaco materno de 30% a 40% acima do normal, na 27a semana de gestação; então, por razões inexplicadas, o débito cardíaco diminui até pouco acima do normal durante as últimas oito semanas de gravidez, independentemente do elevado fluxo sanguíneo uterino, indicando que o fluxo sanguíneo noutros tecidos possa ser reduzido. Pré-eclâmpsia e Eclâmpsia Cerca de 5% de todas as gestantes apresentam hipertensão induzida pela gravidez , que é um rápido aumento da pressão arterial em níveis hipertensivos nos últimos meses de gravidez. Isso também está associado à perda de grande quantidade de proteína na urina. Essa condição é denominada pré-eclâmpsia ou toxemia gravídica e se caracteriza por retenção excessiva de sal e água pelos rins maternos e pelo ganho de peso e desenvolvimento de edema e hipertensão na mãe. Além disso, há comprometimento da função do endotélio vascular, ocorrendo espasmo arterial em muitas partes do organismo materno, mais particularmente nos rins, cérebro e fígado. Tanto o fluxo sanguíneo renal quanto a filtração glomerular são menores, exatamente em oposição às mudanças que ocorrem nas gestantes normais. Esses efeitos renais incluem ainda espessamento dos tufos glomerulares, contendo depósito proteico nas membranas basais. Há ainda evidências de que a pré-eclâmpsia seja desencadeada por suprimento insuficiente de sangue à placenta , resultando na liberação pela placenta de substâncias que causam disfunção difusa do endotélio vascular materno. Há ainda evidências de que a pré-eclâmpsia seja desencadeada por suprimento insuficiente de sangue à placenta , resultando na liberação pela placenta de substâncias que causam disfunção difusa do endotélio vascular materno. Muito embora os fatores que ligam o menor fornecimento sanguíneo placentário à disfunção do endotélio materno ainda sejam incertos, alguns estudos experimentais sugerem um papel para os níveis elevados de citocinas inflamatórias como o fator de necrose tumoral a e a interleucina 6. Os fatores placentários que impedem a angiogênese (crescimento de vasos sanguíneos) também têm mostrado contribuição no aumento de citocinas inflamatórias e pré-eclâmpsia. Eclâmpsia é um grau extremo de pré-eclâmpsia, caracterizada por espasmo vascular por todo o corpo; convulsões clônicas na mãe, às vezes seguidas por coma; grande redução do débito renal; disfunção hepática; geralmente hipertensão grave; e toxemia generalizada. Geralmente, ocorre pouco antes do nascimento do bebê.
Não se sabe a causa exata do aumento da atividade uterina, mas pelo menos duas categorias principais de eventos levam às contrações intensas, responsáveis pelo parto: (1) mudanças hormonais progressivas que aumentam a excitabilidade da musculatura uterina; e (2) mudanças mecânicas progressivas.
Maior Proporção de Estrogênios em Relação à Progesterona. A progesterona inibe a contratilidade uterina durante a gravidez, ajudando, assim, a evitar a expulsão do feto. Por sua vez, os estrogênios têm tendência definida para aumentar o grau de contratilidade uterina, em parte porque elevam o número de junções comunicantes entre as células do músculo liso uterino adjacentes, mas também devido a outros efeitos pouco entendidos ainda. A Ocitocina Causa Contração do Útero.
Essa prolactina age nas mamas maternas para manter as glândulas mamárias secretando leite nos alvéolos para os períodos de amamentação subsequentes. Se o pico de prolactina estiver ausente, ou for bloqueado em decorrência de dano hipotalâmico ou hipofisário, ou se a amamentação não prosseguir, as mamas perdem a capacidade de produzir leite dentro de mais ou menos uma semana. O Hipotálamo Secreta o Hormônio Inibidor da Prolactina A Supressão dos Ciclos Ovarianos Femininos na Nutriz Por Muitos Meses Após o Parto A razão disso parece ser que os mesmos sinais neurais das mamas para o hipotálamo que provocam a secreção de prolactina durante o ato de sugar — seja devido aos sinais nervosos ou devido a efeito subsequente de mais prolactina — inibem a secreção do hormônio liberador da gonadotropina pelo hipotálamo. Isto, por sua vez, suprime a formação dos hormônios gonadotrópicos hipofisários — hormônio luteinizante e hormônio folículo-estimulate. Entretanto, após vários meses de lactação, em algumas mulheres, especialmente naquelas que amamentam seus bebês apenas parte do tempo, a hipófise começa a secretar hormônios gonadotrópicos suficientes para restabelecer o ciclo sexual mensal, embora a amamentação continue. O PROCESSO DE EJEÇÃO (OU “DESCIDA”) NA SECREÇÃO DE LEITE — A FUNÇÃO DA OCITOCINA Quando o bebê suga, ele não recebe quase nenhum leite por mais ou menos 30 segundos. Primeiramente, é preciso que impulsos sensoriais sejam transmitidos através dos nervos somáticos dos mamilos para a medula espinal da mãe e, então, para o seu hipotálamo, onde desencadeiam sinais neurais que promovem a secreção de ocitocina , ao mesmo tempo em que causam secreção de prolactina. A ocitocina é transportada no sangue para as mamas, onde faz com que as células mioepiteliais (que circundam as paredes externas nos alvéolos) se contraiam, assim transportando o leite dos alvéolos para os ductos, sob uma pressão de +10 a 20 mmHg. Em seguida, a sucção do bebê fica efetiva em remover o leite. A Inibição da Ejeção de Leite. Um problema particular na amamentação vem do fato de que diversos fatores psicogênicos ou até mesmo a estimulação generalizada do sistema nervoso simpático em todo o corpo materno possam inibir a secreção de ocitocina e, consequentemente, deprimir a ejeção de leite. Anticorpos e Outros Agentes Anti-infecciosos no Leite. Não só o leite fornece ao recém-nascido os nutrientes adequados, como também proporciona uma proteção importante contra infecções. Por exemplo, vários tipos de anticorpos e outros agentes anti-infecciosos são secretados no leite, em conjunto com outros nutrientes. Além disso, diversos tipos de leucócito são secretados, incluindo neutrófilos e macrófagos , alguns dos quais são especialmente letais a bactérias que poderiam causar infecções mortais aos recém-nascidos.