
























Estude fácil! Tem muito documento disponível na Docsity

Ganhe pontos ajudando outros esrudantes ou compre um plano Premium


Prepare-se para as provas
Estude fácil! Tem muito documento disponível na Docsity
Prepare-se para as provas com trabalhos de outros alunos como você, aqui na Docsity
Os melhores documentos à venda: Trabalhos de alunos formados
Prepare-se com as videoaulas e exercícios resolvidos criados a partir da grade da sua Universidade
Responda perguntas de provas passadas e avalie sua preparação.

Ganhe pontos para baixar
Ganhe pontos ajudando outros esrudantes ou compre um plano Premium
Comunidade
Peça ajuda à comunidade e tire suas dúvidas relacionadas ao estudo
Descubra as melhores universidades em seu país de acordo com os usuários da Docsity
Guias grátis
Baixe gratuitamente nossos guias de estudo, métodos para diminuir a ansiedade, dicas de TCC preparadas pelos professores da Docsity
artigo cientifico de cancer do CU
Tipologia: Notas de estudo
1 / 37

Esta página não é visível na pré-visualização
Não perca as partes importantes!






























BOA LEITURA!
■ INTRODUÇÃO
O câncer de colo do útero é o quarto tumor mais comum em mulheres no mundo, com uma taxa de 7,9%. No Brasil, são estimados 16.370 casos novos de câncer para cada ano do biênio 2018–2019, com um risco estimado de 15,43 casos a cada 100 mil mulheres, sendo o câncer do colo do útero o terceiro tumor mais frequente. 1 Nos países com programas de rastreio organizados, que também contemplam o tratamento das lesões precursoras, houve um declínio na incidência e na mortalidade causada pela doença invasora. 2
A história natural do carcinoma é insidiosa, levando de 3 a 12 anos até que se instale o tumor invasor, o que demonstra ser possível uma intervenção nas formas pré-invasivas da doença.
Com a implementação dos programas de rastreio do câncer do colo do útero, as taxas de detecção do carcinoma de vagina, principalmente as suas formas precursoras, registraram um aumento. A detecção precoce de uma enfermidade pode alterar sua história natural, diminuindo a taxa de mortalidade e morbidade associada ao seu curso, com consequente diminuição dos gastos com o tratamento da doença.
A prevenção divide-se em primária, secundária e terciária, tendo cada etapa aspectos bem definidos:
■ prevenção primária atua removendo os fatores causais da doença, provendo a saúde e atuando na proteção específica, como a vacinação; ■ prevenção secundária inclui as ações que visam à detecção e ao tratamento precoce de uma enfermidade, limitando a sua morbidade; ■ prevenção terciária é um conjunto de ações que visa agilizar o processo de diagnóstico do câncer nas mulheres que já apresentam os sintomas.
|^ PROAGO
|^ Ciclo 16
|^ Volume 3
|
■ ESQUEMA CONCEITUAL
Conclusão
Caso clínico
Colposcopia Histopatologia Biologia molecular
Citologia Métodos propedêuticos para rastreamento e diagnóstico do câncer
Neoplasia intraepitelial cervical
Introdução
Tratamento
Excisão da zona de transformação de tipo 3 com eletrodo reto (SWETZ) Excisão da zona de transformação de tipo 3 com bisturi a frio
Seguimento pós-tratamento
Excisão da zona de transformação de tipo 1 e 2 com alça semicircular de alta frequência
Comparação entre os métodos de cirurgia de alta frequência e bisturi a frio
Neoplasia intraepitelial vulvar
Neoplasia intraepitelial vulvar diferenciada
Seguimento
Lesão intraepitelial escamosa de alto grau da vulva (neoplasia intraepitelial vulvar usual)
Terapias ablativas Tratamento tópico Terapia combinada
Terapias excisórias
Tratamento
Carcinogênese no trato genital inferior
Infecção pelo papilomavírus humano
História natural da infecção pelo papilomavírus humano
Tratamento ablativo Tratamento clínico
Tratamento cirúrgico Neoplasia intraepitelial vaginal Modalidades de tratamento
|^ PROAGO
|^ Ciclo 16
|^ Volume 3
|
■ CARCINOGÊNESE NO TRATO GENITAL INFERIOR
A seguir, são descritos os mecanismos relativos à carcinogênese no TGI.
Para desenvolver o câncer cervical ou as lesões precursoras, é necessária uma infecção persistente por papilomavírus humano (HPV) de alto risco, sendo os tipos 16 e 18 responsáveis por cerca de 70% de todos os cânceres cervicais. 3
O HPV tipo 16 é o mais carcinogênico, responsável por cerca de 55 a 60% de todos os cânceres cervicais, e tem sido detectado em 24% das mulheres infectadas por HPV. 3
O HPV tipo 18 é o segundo mais carcinogênico, representa 10 a 15% dos cânceres do colo do útero, e é encontrado em cerca de 9% das mulheres com HPV. Aproximadamente, outros 10 tipos de HPV de alto risco respondem por 25 a 35% das demais neoplasias cervicais. 3
O HPV, vírus que contém um genoma circular de ácido desoxirribonucleico (DNA) de cadeia dupla, infecta as células epiteliais e depende da diferenciação dessas células para completar seu ciclo de vida. O vírus chega à camada basal das células epiteliais através de microtraumas da superfície epitelial. As etapas subsequentes no ciclo de vida do vírus são estabelecimento, manutenção, produção. 3
A história natural do HPV pode ser resumida em duas fases: infecciosa ou produtiva e persistente. 4
A fase infecciosa resulta em mudanças celulares, incluindo proliferação das células basais resultante da expressão do produto gênico de E6 e E7, bem como alterações citopáticas, como halos perinucleares causados pela expressão de E4. As alterações citopatológicas manifestam-se como lesão intraepitelial escamosa de baixo grau (em inglês, low-grade squamous intraepithelial lesion [LSIL]) e as histopatológicas, como neoplasia intraepitelial cervical grau 1 (NIC 1). Como essas lesões iniciais podem ser pequenas, e a citopatologia é relativamente insensível, nem todas as lesões produtivas são identificadas. As infecções produtivas também podem se desenvolver e regredir entre as triagens e não serem detectadas. 4
A fase de infecção persistente por HPV de alto risco consiste no verdadeiro risco de lesão pré-câncer, com considerável potencial de progressão quando não tratada, sendo representada citopatologicamente pelas lesões intraepiteliais escamosas de alto grau (em inglês, high-grade squamous intraepithelial lesions [HSILs]) e histopatologicamente por NIC 2 e NIC 3.^4
PREVENÇÃO SECUNDÁRIA DO CÂNCER NO TRATO GENITAL INFERIOR
|
O ideal é tratar qualquer cervicite ou leucorreia previamente ao exame, mas nenhuma coleta deve ser adiada diante de leucorreia inespecífica ou sangramento inesperado, uma vez que esses sintomas podem estar relacionados com câncer do colo do útero ou TGI.^7
Como a presença de células escamosas varia ao longo da vida, é indispensável relatar informações ao patologista, tais como,
■ idade; ■ data da última menstruação; ■ status menopausal; ■ gravidez; ■ uso de contraceptivos; ■ uso de dispositivo intrauterino; ■ história de sangramento uterino em investigação; ■ história prévia de citológicos alterados.
Na citologia, a espátula de Ayre (de madeira ou de plástico) é projetada para se encaixar adequadamente ao contorno do colo do útero e acessar a junção escamocolunar (JEC), a zona de transformação (ZT) e o canal endocervical distal. Após a obtenção da amostra com a espátula, deve-se inserir a escova no canal endocervical, até que as cerdas distais se mantenham visíveis no (estejam no nível do) orifício externo. Assim, evita-se a coleta de células do segmento inferior do útero, as quais podem ser confundidas com células cervicais atípicas. 6,
Imediatamente, após a coleta, o material colhido deve ser aplicado, em monocamada, na lâmina (girar a escova endocervical horizontal à lâmina e a amostra ectocervical em sentido perpendicular) e fixado com fixador ou em etanol 95%. Não se deve deixar o material coletado secar no ar. O componente da amostra endocervical secará primeiro do que o componete da espátula. 6,
As gestantes, especialmente após o segundo trimestre, geralmente terão ZT visível. Logo, a amostragem cuidadosa com a espátula obterá, adequadamente, material da ZT.^6
A citologia em base líquida ( ThinPrep) foi introduzida em 1996 e aprovada pela Food and Drug Administration (FDA). Subsequentemente, surgiram os sistemas SurePath e MonoPrep , que obtiveram aprovação da FDA em 1999 e 2006, respectivamente. Esses sistemas surgiram para tentar melhorar a sensibilidade da ciotologia convencional, com a capacidade de fazer a testagem molecular para HPV. 6,
Na citologia em base líquida, a escova deve ter sua porção central e mais longa inserida no orifício endocervical. Uma pressão delicada deve ser aplicada sob o colo para que as cerdas flexionem. Deve-se, então, rodar a escova no mesmo sentido cinco vezes. A escova pode ser usada em grávidas. 6,
Na técnica ThinPrep , a extremidade distal da escova coletora deve ser agitada dentro do frasco e, depois, descartada. Na tecnologia SurePrep , a extremidade final da escova é enviada junto com o frasco/solução fixadora.6,
As diretrizes brasileiras para rastreamento do câncer do colo do útero 1 preconizaram que o rastreio do câncer e de suas lesões precursoras seja trienal, após dois exames citopatológicos anuais normais.
PREVENÇÃO SECUNDÁRIA DO CÂNCER NO TRATO GENITAL INFERIOR
|
A população alvo para rastreamento do câncer do colo do útero deve ser dos 25 aos 64 anos de idade. As pacientes com 64 anos de idade, sem história de doença neoplásica pré-invasiva e com dois resultados citológicos negativos nos últimos 5 anos podem ter seu rastreio interrompido.
Pacientes de 64 anos e que nunca realizaram exame citopatológico devem coletar duas citologias com intervalo de 1 a 3 anos. Se ambas forem negativas, não precisarão de exames adicionais. As pacientes submetidas à histerectomia total e sem história de doença neoplásica pré-invasiva também estarão dispensadas do rastreamento.
Com vistas à padronização, os laudos da citologia devem seguir a Nomenclatura de Bethesda (Quadro 1).
Quadro 1
Anormalidades de células epiteliais
Células escamosas
■ ■ ASCUS ■ ■ ASC-H ■ ■ LSIL abrangendo HPV/displasia leve/NIC 1 ■ ■ HSIL abrangendo displasia moderada e grave, CIS, NIC 2 e NIC 3 ■ ■ Carcinoma de células escamosas
Células glandulares
■ ■ Atípicas:
ASCUS (em inglês, atypical squamous cells of undetermined significance): células escamosas atípicas de significado indeterminado; ASC-H (em inglês, atypical squamous cells-cannot exclude high-grade squamous intraepithelial lesion): células escamosas atípicas — não é possível excluir lesão de alto grau; CIS: carcinoma in situ; SOE: sem outras especificações; AIS: adenocarcinoma in situ. Fonte: Adaptado de Health Organization (2019). 8
Quando anormalidades são detectadas durante o rastreamento, a avaliação visual ampliada do colo do útero (colposcopia) tem papel importante no algoritmo para diagnosticar câncer ou pré-câncer do colo do útero. 5
A colposcopia é considerada a técnica mais sensível para detectar lesões invasivas e pré-invasivas do colo do útero. A sensibilidade para o referido método é de 70%. 5
O exame colposcópico implica avaliação sistemática do TGI, com ênfase especial no epitélio e nos vasos sanguíneos do estroma subjacente. O principal papel da colposcopia é localizar a área da lesão e direcionar as biópsias para as áreas suspeitas. Para que isso seja possível, é preciso delimitar a ZT.
|^ PROAGO
|^ Ciclo 16
|^ Volume 3
|
Posteriormente, o Índice de Reid foi modificado, havendo a eliminação dos aspectos relacionados à coloração pelo iodo, que já havia sido excluída por vários colposcopistas, e os três aspectos restantes receberam pontuação de 0 a 3. As áreas com achados suspeitos ou com alto escore para lesão de alto grau devem sofrer biópsia. A conduta, nessas situações, será determinada a partir da impressão colposcópica e da histopatologia incisional. 5
Após o Índice de Reid, foi desenvolvido o Swede Score , índice colposcópico que incluíu o tamanho da lesão nas variáveis do Índice de Reid. O Swede Score tem especificidade de 90% para excluir lesão superior ou igual a NIC 2 quando o escore for inferior a 5. Também foi verificado que 70% das lesões maiores revelam escore mínimo de 2 pontos, resultando em lesões histopatológicas superiores ou iguais à NIC 2.^10
O conceito de doença pré-invasiva do colo foi introduzido em 1947, quando se reconheceu que poderiam ser identificadas alterações epiteliais que possuíam aparência de câncer invasivo, mas eram limitadas ao epitélio. Estudos subsequentes mostraram que, caso as lesões não fossem tratadas, poderiam evoluir para câncer cervical. 11
As características mais significativas para o diagnóstico histológico de NIC incluem imaturidade celular, desorganização celular, anormalidades nucleares e aumento da atividade mitótica. O grau de atividade mitótica, a proliferação celular imatura e a atipia nuclear identificam o grau de neoplasia. Se houver mitoses e células imaturas apenas no terço inferior do epitélio, a lesão é designada como NIC 1. O envolvimento dos terços médio e superior é diagnosticado como NIC 2 e NIC 3, respectivamente.^11
A nomenclatura histopatológica segue a Classificação Histológica de Richardt, de 1967. As lesões intraepiteliais escamosas de baixo grau incluem NIC 1 (displasia leve) e as alterações do HPV, denominadas de atipia coilocitótica. A categoria HSIL inclui NIC 2 e NIC 3 (displasia moderada, displasia grave e CIS).
Outro progresso importante no rastreamento de câncer cervical foi a introdução da testagem molecular para DNA de HPV de alto risco no tratamento de pacientes com anormalidades epiteliais cervicais. O vírus pode ser testado a partir da amostra coletada para citologia líquida. 6 Trata-se de uma técnica mais sensível do que a citologia. O teste deve ser usado em um cenário de rastreamento organizado. 12
A testagem molecular para DNA de HPV de alto risco é uma técnica melhor do que a citologia para identificar lesões glandulares (adenocarcinoma).^12
|^ PROAGO
|^ Ciclo 16
|^ Volume 3
|
Em 2018, um grupo de revisores normatizou, no Brasil, o uso do teste de DNA-HPV no rastreamento do câncer do colo do útero, no seguimento de mulheres com atipias citológicas ou em pós-tratamento de NIC. As diretrizes são as seguintes:^12
■ o teste de DNA-HPV pode ser usado como rastreamento primário (alternativa à citologia) em mulheres com 30 anos de idade ou mais. Quando negativo, pode ser repetido em 5 anos; ■ quando o teste de DNA-HPV for positivo para HPV oncogênico, uma citologia deve ser realizada para evitar encaminhamentos exagerados para a colposcopia. Porém, quando a genotipagem estiver disponível e o teste DNA-HPV for positivo para os tipos 16 e 18, a mulher deve ser encaminhada para a colposcopia. ■ mulheres com resultado citológico de ASCUS e com 30 anos de idade ou mais podem realizar, em 6 meses, teste de DNA-HPV como alternativa a uma nova citologia; ■ mulheres com resultado citológico de LSIL e com 30 anos ou mais podem realizar teste de DNA-HPV para seleção de encaminhamento à colposcopia; ■ em mulheres com resultados citológicos de ASC-H e HSIL, com colposcopia normal, um teste DNA-HPV negativo, teoricamente, elimina a possibilidade de lesões precursoras ou doenças invasivas; ■ em mulheres com resultados citológicos de atipia de células glandulares (AGC) e AIS, com colposcopia normal, um teste DNA-HPV negativo significa baixa probabilidade de doença cervical e impõe a necessidade de investigar endométrio e outros órgãos pélvicos; ■ o teste de DNA-HPV pode ser usado no seguimento de tratamento de lesões NIC 2/3 e AIS para excluir doença residual ou recorrente, e é recomendado que seja realizado em 6 e 12 meses após o tratamento.
A) O carcinoma apresenta história natural insidiosa, levando de 2 a 8 anos até que se instale o tumor invasor. B) Ações que visam à detecção e ao tratamento precoce de uma enfermidade, limitando a sua morbidade, integram a prevenção primária. C) Remoção dos fatores causais da doença, promoção da saúde e atuação na proteção específica, como a vacinação, são características da prevenção secundária. D) Um conjunto de ações que objetiva agilizar o processo de diagnóstico de câncer nas mulheres que já apresentam os sintomas compõe a prevenção terciária. Resposta no final do capítulo
A) Fase infecciosa. B) Fase de estabelecimento. C) Fase de infecção persistente. D) Fase produtiva. Resposta no final do capítulo
PREVENÇÃO SECUNDÁRIA DO CÂNCER NO TRATO GENITAL INFERIOR
|
■ NEOPLASIA INTRAEPITELIAL CERVICAL
A seguir, são descritos os principais aspectos relativos à NIC.
A prevenção do câncer do colo do útero é feita por meio de programas de rastreio organizado, os quais podem detectar a doença na fase precursora e tratá-la antes do desenvolvimento do carcinoma invasor.
A NIC é a condição pré-maligna do colo do útero que, em uma pequena proporção dos casos, poderá progredir se não for tratada adequadamente.
As lesões precursoras do câncer cervical foram inicialmente denominadas como displasia leve , moderada e acentuada. A partir de 1988, uma nova nomenclatura foi introduzida, conhecida como sistema Bethesda, que foi revisado em 1991 e em 2001. Nesse sistema, foi introduzida uma nomenclatura para os achados citológicos (SIL) e outra para os achados histológicos (NIC).^13
As NICs são classificadas em três categorias, a saber:
■ NIC 1 — é uma lesão de baixo grau, que está presente no terço inferior do epitélio e apresenta atipias celulares de grau leve. É considerada a manifestação citológica da infecção pelo HPV. ■ NIC 2 — pode ser considerada uma lesão de alto grau. Compromete os dois terços do epitélio. Essa categoria possui moderada reprodutibilidade interobservador; ■ NIC 3 — é a verdadeira precursora do câncer do colo do útero, apresentando alterações nos três terços do epitélio, com perda total de polaridade e monotonia celular.
Em 2012, foi introduzida outra nomenclatura para a classificação das NICs, denominada Lower Anogenital Squamous Terminology (LAST), sistema que classifica os achados de histopatologia da mesma maneira que os da citologia. Assim, a NIC 1 é referida como LSIL. A NIC 2 é classificada de acordo com a positividade ou não pelo p16, pois, além de ser pouco reprodutível, é sabidamente heterogênea. Em alguns casos, tem comportamento de uma NIC 1, enquanto, em outros, de uma NIC 3, ou seja, uma verdadeira precursora do carcinoma do colo do útero. A lesão que se cora pelo p16 é considerada HSIL, e a lesão p16 negativa é classificada como lesão de baixo grau.^13
A lesão de baixo grau é considerada o reflexo da infecção pelo HPV, sendo muito comum em mulheres abaixo dos 30 anos de idade. No Brasil, a prevalência dessa lesão na citologia é de 0,8% dos exames citológicos e de 27,6% dentre as citologias alteradas. 1
O potencial de regressão das lesões de baixo grau é grande, como foi demonstrado por Bansal e colaboradores, que, em um estudo com 680 mulheres portadoras de NIC 1, segundo biópsia, e que foram seguidas por um período de 12 meses, encontraram, na citologia realizada nos 6 meses, os seguintes dados:^14
■ 49% tiveram o exame citológico negativo; ■ 35% apresentaram persistência da doença; ■ 7% progrediram para HSIL.
PREVENÇÃO SECUNDÁRIA DO CÂNCER NO TRATO GENITAL INFERIOR
|
Na visita correspondente a 12 meses, dentre as mulheres que tinham citologia negativa aos 6 meses, observou-se que 14
■ 80% permaneceram com resultados negativos; ■ 17% apresentaram LSIL; ■ 4% HSIL.
Dentre as pacientes que tinham persistência de LSIL aos 6 meses, ficou demonstrado que^14
■ 50% regrediram; ■ 46% permaneceram com LSIL; ■ 4% progrediram para HSIL.
Como a reprodutibilidade do diagnóstico de lesão de baixo grau é pobre, muitos casos rotulados como HSIL não seriam consequência de uma progressão da doença, e sim de um provável subdiagnóstico de uma lesão de maior gravidade. 14
As lesões de alto grau são diagnosticadas com maior frequência na faixa etária entre 25 e 35 anos, enquanto a doença invasora ocorre cerca de 10 a 13 anos após a detecção das neoplasias precursoras. A incidência estimada nos Estados Unidos é de 4% para NIC 1 e 5% para NIC 2 e 3. No Brasil, cerca de 0,26% das citologias correspondem a HSIL, que está presente em 9,1% dos casos de exames alterados. 1
Os fatores de risco para as NICs são a infecção pelo HPV e os cofatores como tabagismo, uso de anticoncepcionais orais e imunossupressão.
O principal método de prevenção secundária do câncer do colo do útero é o tratamento das lesões intraepiteliais de alto grau. Tanto as pacientes com NIC 2 quanto as portadoras de NIC 3 serão manejadas da mesma maneira em razão da dificuldade de distinção entre os graus histopatológicos das lesões.
Aparentemente, 50% das NICs 2 terão regressão se permanecerem sem tratamento. Em uma metanálise publicada em 2018, que incluiu 3.160 mulheres portadoras de NIC 2, foi observado, após 24 meses, que 50% tiveram regressão da doença, 32% persistiram e 18% progrediram para NIC 3. Em um subgrupo de mulheres com menos de 30 anos de idade, foram encontradas taxas de 60% de regressão, 23% de persistência e 11% de progressão da doença. O risco da perda de seguimento deverá ser levado em conta quando se pretende ter uma conduta mais conservadora.^15
No estudo ALTS, a regressão de NIC 2 foi menor nas lesões positivas para o HPV 16. Quando comparadas as taxas de progressão da NIC 2 com as da NIC 3, foi vista uma maior progressão dessa última, o que foi explicado pelo fato de os tipos de HPV mais comuns na NIC 2 serem outros tipos oncogênicos, como 31, 33, 35, 39, 45, 51, 52 e 58, os quais têm uma associação mais fraca com a doença invasora do que os tipos 16 e 18, que são mais comuns na NIC 3. 16
Nos casos de NIC 3, está estimada uma taxa de regressão espontânea entre 32 e 47%, enquanto 12 a 40% das pacientes progredirão para carcinoma invasor se não forem submetidas a tratamento. Em razão da grande taxa de progressão, a conduta expectante não é recomendada. 16
|^ PROAGO
|^ Ciclo 16
|^ Volume 3
|
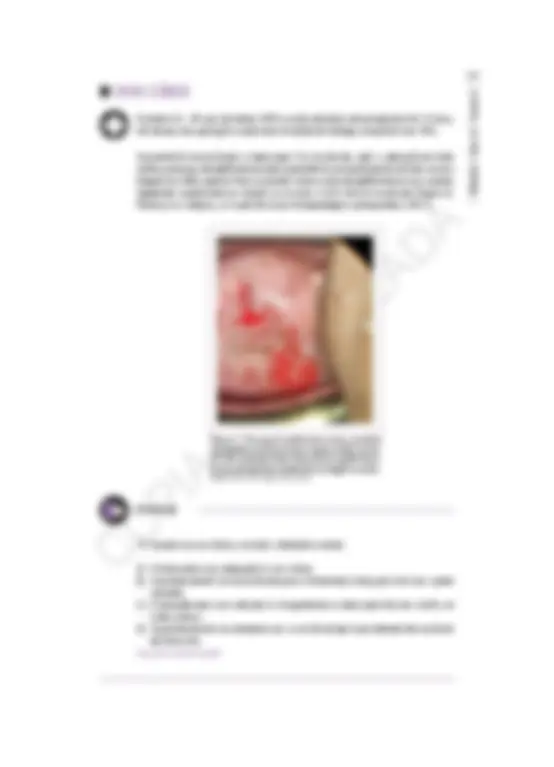
Figura 1 — ZT 1: componente ectocervical totalmente visível, que pode ser pequeno ou grande. Fonte: Arquivo de imagens de Cibele Feroldi Maffini.
Figura 2 — ZT 2: componente endocervical totalmente visualizado; pode ter um componente ectocervical pequeno ou grande. Fonte: Cedida por Cibele Feroldi Maffini.
Figura 3 — ZT 3: componente endocervical não totalmente visível; pode ter um componente ectocervical pequeno ou grande. Fonte: Cedida por Cibele Feroldi Maffini.
|^ PROAGO
|^ Ciclo 16
|^ Volume 3
|
Para cada tipo de ZT, há um tipo de excisão, a saber:^9
■ excisão do tipo 1 — corresponde a uma retirada totalmente ectocervical, ou seja, é realizada na ZT 1; ■ excisão de tipo 2 — compreende a retirada de uma pequena porção de epitélio do canal cervical, ou seja, é empregada na ZT 2; ■ excisão de tipo 3 — corresponde àquela em que a retirada do epitélio endocervical será maior e mais longa, adentrando o canal cervical em seu limite superior, sendo utilizada na ZT 3.
A excisão de tipo 3 é mais apropriada no manejo das lesões glandulares, na doença microinvasiva e nas pacientes que já foram tratadas previamente. 9
A excisão de cada tipo de ZT está associada a uma determinada técnica, como também apresenta riscos diferentes em relação à morbidade. 9
As duas técnicas excisionais mais utilizadas no tratamento das lesões intraepiteliais cervicais são a cirurgia de alta frequência (CAF) e a ressecção com bisturi a frio.
A excisão da ZT 1 e da ZT 2, com alça semicircular de alta frequência, é a modalidade de tratamento excisional mais empregada atualmente. Esse procedimento poderá ser tanto diagnóstico como terapêutico; porém, o foco principal para a sua utilização é a terapia. Uma de suas principais vantagens é poder ser realizado ambulatorialmente. Anteriormente ao procedimento, uma colposcopia deverá ser realizada para a visualização da lesão e a demarcação da ZT.
Para um manejo eficaz, a ZT deve ser removida em sua totalidade. A retirada somente da área mais atípica do colo não é recomendada em razão da alta taxa de recorrência. 19
A exérese deverá ser realizada em um só fragmento, e todo cuidado deverá ser feito para evitar o dano térmico. O procedimento hemostático é obtido pela fulguração dos pontos sangrantes presentes na cratera decorrente da exérese.
A cicatrização é realizada por meio da reepitelização secundária , que tem, como resultado, um colo com JEC visualizada, permitindo uma boa coleta da citologia e a realização de um exame colposcópico adequado. A taxa de cura da excisão da ZT 1 e da ZT 2 com alça semicircular de alta frequência é de 95%, a mesma obtida por outros métodos, como o realizado com bisturi ou laser.
As principais indicações da cirurgia com a alça de alta frequência são as lesões presentes na ZT 1 e na ZT 2 e o método ver x tratar.
PREVENÇÃO SECUNDÁRIA DO CÂNCER NO TRATO GENITAL INFERIOR
|
Na excisão da ZT 3 com o eletrodo reto, as complicações poderão ocorrer em 5,6% dos procedimentos para tratamento das lesões de alto grau do colo do útero. Cerca de 1 em 500 mulheres terão complicações hemorrágicas, principalmente sangramento. Poderá também haver relato de dor, infecção, estenose e danos ao futuro obstétrico.
A excisão de tipo 3 com bisturi a frio está indicada para pacientes que apresentam uma ZT 3, principalmente quando há suspeita de doença microinvasora e nas lesões glandulares.
O procedimento de excisão de tipo 3 com bisturi a frio é realizado em centro cirúrgico sob raquianestesia.
A principal complicação da excisão de tipo 3 com bisturi a frio é o sangramento no transoperatório ou no pós-operatório imediato.
O coto cirúrgico deverá ser visualizado à procura de pontos de sangramento, poderá ser realizada a cauterização desses pontos. Na presença de sangramento arterial, deverão ser feitos pontos hemostáticos com fio de vicryl 0 em forma de chuleio. Um tampão vaginal deverá permanecer durante 24 horas. Outras complicações são a dor em fossa ilíaca, a infecção e, tardiamente, o aparecimento de estenose e repercussões no futuro obstétrico, como maior taxa de PP e BP ao nascer.
Nenhum dos métodos (CAF e bisturi a frio) mostra superioridade quanto à eficácia e à segurança.^23
Comparado com o cone com bisturi, a CAF tem
■ tempo operatório mais curto (média de 9,5 minutos; 95%, intervalo de confiança [IC]: 6,4–12, minutos); ■ menor taxa de sangramento (média de 42,4mL; 95%, IC: 21,3–106mL); ■ estadia hospitalar menor (média de 1,5 dias; 95%, IC: 1,1–1,8 dias).
A incidência de sangramento pós-operatório não foi significativa entre os procedimentos. A presença de infecção pós-operatória foi relatada mais frequentemente após a CAF (0,2 x 2%, risco relativo [RR]: 0,31; 95%, IC: 0,08–1,10).
A taxa de estenose referente ao procedimento com a CAF é de 4% e de 8,3% no cone com bisturi. Porém, a CAF apresenta um risco maior de doença pós-tratamento (RR 2,3; 95% IC: 1,0–5,5) em relação ao cone com bisturi.^24
A conização com o bisturi está relacionada a um maior dano no futuro obstétrico da paciente.^21 As evidências dão suporte para que a escolha entre a CAF e o bisturi não seja puramente técnica, e sim com a avaliação dos benefícios a curto e a longo prazo, bem como das complicações que ainda não estão inteiramente elucidadas pela literatura.
PREVENÇÃO SECUNDÁRIA DO CÂNCER NO TRATO GENITAL INFERIOR
|
Tão importante quanto o tratamento das lesões é o seguimento após a terapêutica, que deverá se basear no status das margens.
No caso de comprometimento das margens, a paciente deverá ser seguida com citologia e colposcopia semestralmente, durante 24 meses. Se esses exames forem negativos, ela deverá repeti-los anualmente, durante cinco anos e, depois, trienalmente. No caso de margens livres, deverá ser feito um acompanhamento com citologia semestral durante 12 meses e, depois, anualmente, durante 5 anos. Se os exames permanecerem negativos, a paciente voltará ao rastreio trienal.
I — Lesão de baixo grau que está presente no terço inferior do epitélio e apresenta atipias celulares de grau leve, a NIC 1 é considerada a manifestação citológica da infecção pelo HPV. II — A NIC 2, que pode ser considerada uma lesão de grau moderado, compromete dois terços do epitélio e possui alta reprodutibilidade interobservador. III — Verdadeira precursora do câncer do colo do útero, a NIC 3 apresenta alterações nos três terços do epitélio, com perda total de polaridade e monotonia celular.
Quais estão corretas?
A) Apenas a I e a II. B) Apenas a I e a III. C) Apenas a II e a III. D) A I, a II e a III. Resposta no final do capítulo
( ) Muito comum em mulheres acima dos 30 anos de idade, a lesão de baixo grau é considerada o reflexo da infecção pelo HPV. ( ) No Brasil, a prevalência da lesão de baixo grau é de 0,8% dos exames citológicos e de 27,6% dentre as citologias alteradas. ( ) As lesões de baixo grau apresentam potencial de regressão reduzido. ( ) Por ser a reprodutibilidade do diagnóstico de lesão de baixo grau pobre, muitos casos rotulados como HSIL seriam consequência de um provável subdiagnóstico de uma lesão de maior gravidade.
|^ PROAGO
|^ Ciclo 16
|^ Volume 3
|